論文紹介
大豆由来のホスファチジルセリン/ホスファチジン複合体(PAS)は、慢性的にストレスをうけた男性被験者における視床下部-下垂体-副腎軸のストレス反応性を正常化する
今回は
(論題)
A soy-based phosphatidylserine /phosphatidic acid complex(PAC) normalizes the stress reactivity of hypothalamus-pituitary-adrenal-axis in chronically stressed male subjects:a randomized,placeb-controlled study
(論題訳)
大豆由来のホスファチジルセリン/ホスファチジン複合体(PAS)は、慢性的にストレスをうけた男性被験者における視床下部-下垂体-副腎軸のストレス反応性を正常化する:無作為プラセボ対照研究
という論文をご紹介いたします。
はじめに…
これまでの研究でホスファチジン酸(以下PA)(*1)は
①動物実験で胃腸障害を予防・回復する。
②骨格筋量を増加させる。
ホスファチジルセリン(以下PS)は
①記憶・学習・気分・ストレス管理を改善させる。
②急性の肉体ストレス・精神的ストレスに対しACTHとコルチゾールの反応を減少させる。
③炎症性神経変性事象の予防・双極性および大うつ病障害等精神障害の改善と関連している。
ことが示唆されてきました。
上記に加えさらにPAとPSの複合体(ホスファチジン酸複合体(以下PAS)は)コルチゾールレベルを低下させ、急性の社会的ストレス下での幸福を高めることが近年の研究で示されました。
*1.ホスファチジン酸(PA)…細胞膜の重要な構成要素でホスファチジルセリンやホスファチジルコリン等他の脂質の生合成における前駆体としての利用等の役割を持つ。
この研究は
以前の研究で見つかったPAS400の容量のHPAA(*2)標準化効果を確認する必要があり、またPAS200のより少ない投与量でも同様の効果が観察され得るかを確認する必要がある。
との考えから行われました。
*2.HPAA…視床下部-下垂体-副腎軸のこと。詳しい内容の<はじめに>部分に詳細を記載しております。
この実験により
PASは肉体的ストレスと精神的ストレスの両方を軽減するための安全かつ効果的な補足物である
ことが分かりました。
詳しい内容は以下に記載致しますのでご興味のある方はどうぞご覧くださいませ。
<はじめに~ストレス反応とは~>
●ストレス…内分泌系・自律神経系を介して中枢神経系におけるストレス反応ネットワークや抹消器官とのクロストークに影響を与える個々の応答のこと。
●視床下部-下垂体-副腎軸(HPAA(*2))は生物の様々な適応プロセスにおいて重要な役割を担う。急性ストレス要因に応答して視床下部は副腎皮質刺激ホルモン(以下ACTH)の下垂体からの放出を誘発するコルチコトロピン放出因子を分泌する。ACTHは副腎皮質からのコルチゾール(*3)の放出を促進する。
簡単にまとめると
急性ストレス要因→コルチコトロピン放出因子(視床下部)→ACTH(下垂体)→コルチゾール(副腎皮質)
と放出を促していく。
*3.コルチゾール…副腎皮質から放出される。炭水化物、脂質、タンパク質代謝、免疫系など多くの生理学的昨日に影響を及ぼし中枢神経系のエネルギー供給を高める。
●慢性的な心理的ストレスは心理的および身体的健康障害を伴うHPAAの調節不全を誘発することが示唆されており、ストレス下では※HPAAの二相性反応が観察。
※ストレス下でのHPAA二相性反応:長期の心理的ストレスはHPAAの①過活性をまずはじめに誘発し、その後②低活性化が続く。
①HPAAの過活性が身体に及ぼす影響
うっ血性うつ、不安障害、メタボリックシンドローム…etc
②HPAAの低活性が身体に及ぼす影響
疲労、過敏症、線維筋痛症、関節炎、慢性疲労症…etc
近年の研究で特定の栄養補助食の摂取が上記異常の調整やストレス症候を正常化したと示唆された。
<被験者と実験方法>
1.被験者
20~45歳の健康な男性75名
2.方法
- 低慢性ストレス群と高慢性ストレス群の2群に分け、それぞれを更にプラセボ群・PAS200群・PAS400群の3群に分類。
- 21日間、それぞれプラセボ・PAS200・PAS400のカプセルを毎日摂取。
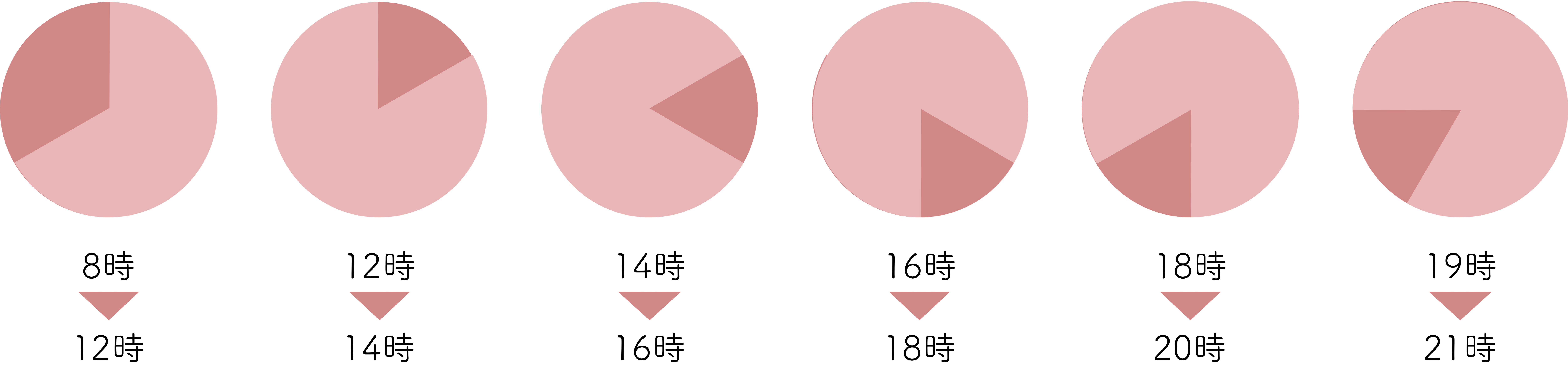
- 血液採取後トリアーソーシャルストレステスト(以下TSST)(*4)を実施。TSSTの前後で心理検査を実施し、更にHPAA活性測定のため唾液および血液をTSSTの前後とテスト中に採取。血液は後にACTH分析にも使用。
- また、自律神経系の測定のため心拍数やパルス通過時間(以下PTT)(*5)も前後に測定した。
- 心理評価もTSST前中後に実施。内容は多次元気分状態アンケート、不安感やストレスレベルの測定。
*4.トリアーソーシャルストレステスト(TSST)…急性心理社会的ストレス状態を誘発するためのストレステスト。HPAAの応答を引き起こすのに最も効果的であり、ストレスや不安に対する個人の感情の強い増加を引き起こす。
*5.パルス通過時間(PTT)…心電図と脳波の測定により決定されるもので、ストレス測定のための適切なパラメータとされている。
<結果>
TSSTにより知覚されるストレス応答はすべての治療群において同様であった。
HPAA反応に対するPASの顕著な応用力減衰効果は高慢性ストレス群での400mg処置群でのみ観察。慢性ストレスがHPAAの過敏性をもたらす場合リン脂質はストレスに対するHPAA応答を緩衝すると予想され得る。
PAS400の効果は内分泌のみで認められたが自律神経ストレス反応では観察されなかった。この結果よりPASは主にHPAA周辺の構成要素をターゲットに効果を発揮する可能性を示した。
<結論>
慢性的にストレスを受けた場合PAS400はコルチゾール応答を正常化スつことでHPAAの急性ストレス要因に対する過敏性を緩衝することが期待される。
心血管疾患、中枢性肥満やメタボリックシンドロームのようなストレスにより上昇したコルチゾールが引き起こすストレス関連障害などへのPASの応用も期待出来る。
肉体的ストレスや精神的ストレスの両方を軽減するための安全かつ効果的な補足物である。
慢性腎不全患者の血中アミノ酸濃度と必須アミノ酸療法の検討
今回は
(論題)
慢性腎不全患者の血中アミノ酸濃度と必須アミノ酸療法の検討
という論文をご紹介いたします。
この研究は
慢性腎不全患者と健常人ではタンパク質代謝(*1)や腎尿細管のアミノ酸動態が全く同一であるか否かが不明であるため、慢性腎不全患者のアミノ酸代謝を検討し現在行われている低たんぱく食のアミノ酸組成について改善することが長期にわたる保存的療法を可能にするのではないか。
上記の考えから行われました。
*1.タンパク質代謝…タンパク質はアミノ酸からできており食事で摂取したタンパク質が小腸でアミノ酸に分解され肝臓に運ばれる。肝臓でこのアミノ酸が様々なタンパク質に合成されそれらは血中に、使われなかったアミノ酸が分解され窒素酸化物→アンモニア→尿素とな尿中に排泄される。この一連の働き。
この実験により
極度の摂取蛋白制限下の慢性腎不全患者に投与した必須アミノ酸はそれに相当する窒素量を含む食事蛋白よりも有効に体蛋白合成に利用され、BUN(*2)値も抑えられることがわかり食事療法のみで管理が困難な症例に適用し得る可能性があることが分かりました。
*2.BUN…血中尿素窒素。正常値は約10-20mg/dl。蛋白質の多い食事等の影響でも数値が上昇することがあるためCre(クレアチニン)等と共に血液検査で腎機能の評価がなされる。
詳しい内容は以下に記載致しますのでご興味のある方はどうぞご覧くださいませ。
<研究対象者・施した処置>
必須アミノ酸溶液の投与
42歳男性、BUN 95mg/dlの慢性腎不全患者
尿及び糞便中の窒素排泄量を摂取窒素量より減じ窒素バランスを求めた。
投与した必須アミノ酸溶液には200ml中アミノ酸10.84g、窒素量として1.42g含有。
組成はイソロイシン・ロイシン・リジン・バリン・メチオニン等9種類のアミノ酸を使用。
<処置前後の変化の確認方法>
必須アミノ酸溶液の投与によるBUN(*2)、血清クレアチニン(*3)、窒素バランスの変化を確認。
*3.クレアチニン(Cre)…主に筋肉に含まれるアミノ酸。特殊な事情がない限り排泄量は一定。食事中のタンパク質量で変動するBUN(*2)とともに血液検査で腎機能の評価がなされ、両者の比較により腎障害の原因がどこにあるのか見当をつける。
<結果>
①アミノ酸溶液の投与前の窒素排泄量は窒素バランス(*4)は負となっているものの投与中に比べ明らかに多量。
→摂取されたアミノ酸がタンパク合成に利用されずに代謝された結果と考えられる。
*4.窒素バランス…食事中の窒素化合物が排泄物中の窒素より多い(正の平衡)か少ない(負の平衡)か。腎臓病では窒素の排泄が悪くなる為、食事中の窒素を減らして(負になるよう)なるべくバランスを取るようにする。
②アミノ酸溶液投与中は窒素バランスが正であるにもかかわらず窒素排泄量が投与前に比べ減少しBUNが上昇していなかった。
→摂取された窒素が効率よく蛋白合成に利用されたと推測。
更にアミノ酸投与期間中は嘔気・食欲不振の改善がされたが体重変動はなく血漿蛋白や赤血球・ヘモグロビン量も不変。
③また、アミノ酸溶液の投与中止後食事蛋白を増量し投与中と等しい窒素摂取量となるようしたがBUNが増加する結果となった。
<結論>
極度の摂取蛋白制限化の慢性腎不全患者に投与した必須アミノ酸はそれに相当する窒素量を含む食事蛋白よりも有効に体蛋白合成に利用されることを知り、さらに食事療法のみで管理困難な症例に適用し得る可能性を得た。
論文紹介
●オメガ3脂肪酸(DHA・DPA・EPA等)
- 2018.04.25
- 14:38
- コメント (0)
犬の腫瘍細胞の増殖及び死に対する分岐鎖アミノ酸の影響
今回は2006年に発表された
(論題)
The effect of Branched-Chain Amino Acids on Canine Neoplastic Cell Proliferationm and Death
(論題訳)
犬の新生物(腫瘍)細胞の増殖及び死に対する分岐鎖アミノ酸の影響
という論文をご紹介いたします。
この研究は
これまでの研究で悪液質(*1)など筋萎縮のモデルにおいて分岐鎖アミノ酸(以下BCAA)が除脂肪体重(筋肉量)を保存するのに役立つと示唆されていました。
なので医師はがん性悪液質で体重維持の為BCAAの使用を提唱することがあるが、その際BCAAが腫瘍細胞に対してどのように影響するのかが大切になる。
との考えから行われました。
*1.悪液質…基礎疾患に関連して生ずる複合的代謝異常の略。脂肪量の減少の有無にかかわらず筋肉量の減少を特徴とする。
悪性腫瘍や白血病等でよく認められる。
この実験により
ロイシン・イソロイシン・バリン・アルギニンを使用した細胞3株(犬骨肉腫細胞、犬気管支肺胞がん細胞、犬腎尿細管上皮細胞)全てにおいて抗増殖作用が認められた。
アルギニンとロイシンにおいて骨肉腫細胞と犬腎尿細管上皮細胞の顕著なアポトーシス(*2)の誘導が認められた。
ロイシンのみ骨肉腫細胞の細胞周期(*3)のG2M期の喪失を示し多くの骨肉腫細胞がS期に停止をした。
ことが分かりました。
*2.アポトーシス…プログラムされた細胞死。
*3.細胞周期…G0期(静止期間)→G1期(DNA合成準備期間)→S期(DNA合成期間)→G2期(分裂準備期間)→M期(有糸分裂期間)→G0期(静止期間)に戻る。
上記の結果を表にまとめたものがこちらです。
| ロイシン | すべて抑制(10mmol/L) | 骨肉腫 | G2M期排除(S期で停止) |
| イソロイシン | すべて抑制(100mmol/L) | - | - |
| バリン | すべて抑制(100mmol/L) | - | - |
| アルギニン | すべて抑制(50mmol/L) | 骨肉腫・MDCK | - |
詳しい内容は以下に記載致しますのでご興味のある方はどうぞご覧くださいませ。
<使用するアミノ酸・細胞>
●細胞
犬骨肉腫細胞
犬気管支肺胞がん細胞
犬腎尿細管上皮細胞(MDCK)
●アミノ酸
アルギニン
BCAA
→ロイシン
→イソロイシン
→バリン
※アルギニンはBCAAではないが、これまで腫瘍細胞を使用した研究で最も集中的に研究されてきたアミノ酸であるため補助的にアルギニンも使用し同様の実験を行った。
<試験内容>
1.細胞崩壊
犬骨肉腫細胞・犬気管支肺胞がん細胞・犬腎尿細管上皮細胞(MDCK)において、それぞれのアミノ酸による増殖抑制効果を調べる。
2.アポトーシス(*2)
犬骨肉腫細胞・犬気管支肺胞がん細胞・犬腎尿細管上皮細胞(MDCK)において、それぞれのアミノ酸によるアポトーシスの対する影響を調べる。
3.フローサイトメトリー(*5)
犬骨肉腫細胞・犬気管支肺胞がん細胞・犬腎尿細管上皮細胞(MDCK)において、それぞれのアミノ酸による細胞の増殖や周期などに与える影響を調べる。
*5.フローサイトメトリー……試料中の細胞の数や生存する細胞の割合、起きさや形状等を測定する手法。短時間で多量の細胞数やその特徴を計測することが可能。
<結果>
1.細胞崩壊
●有効なアミノ酸
すべてのアミノ酸(ロイシン・イソロイシン・バリン・アルギニン)
●抗増殖作用が認められた細胞
すべての細胞(骨肉腫細胞・気管支肺胞がん細胞・MDCK細胞)
●強さ
ロイシン > アルギニン >イソロイシン・バリン
2.アポトーシス
●有効なアミノ酸
ロイシン・アルギニン
●アポトーシスが認められた細胞
骨肉腫細胞・MDCK細胞(アルギニンのみ)
●強さ
アルギニン > ロイシン
3.フローサイトメトリー
●有効なアミノ酸
ロイシン
●細胞周期の以上が認められた細胞
骨肉腫細胞(S期で停止・G2 M期が排除)
上記の結果を表にまとめたものがこちらです。
| ロイシン | すべて抑制(10mmol/L) | 骨肉腫 | G2M期排除(S期で停止) |
| イソロイシン | すべて抑制(100mmol/L) | - | - |
| バリン | すべて抑制(100mmol/L) | - | - |
| アルギニン | すべて抑制(50mmol/L) | 骨肉腫・MDCK | - |
<結論>
BCAAは腫瘍細胞の増殖を抑制する可能性があることが本研究により示唆された。
- 2017.11.14
- 13:35
- コメント (0)
膵臓がんにおけるDHAの抗腫瘍機序
今回は2017年3月にJOURNAL OF CANCER PREVENTIONに掲載された
(論題)
Anti-cancer Mechanism of Docosahexaenoic Acid in Pancreatic Carcinogenesis:A Mini-review
(論題訳)
膵臓がんにおける(ドコサヘキサエン酸)DHAの抗腫瘍機序
というレビュー論文をご紹介いたします。
これまでの疫学的研究ではオメガ3脂肪酸の高い消費は膵臓がんのリスクを低下させること、食餌性魚油の補給は動物モデルにおける膵臓がん発生を抑制すること、DHAは抗腫瘍活性を示すこと、等が示唆されていました。
この論文の結論として
DHAは膵臓がん細胞においてアポトーシス(*1)を誘導することやDHAは血管新生(*2)促進因子の発現を抑制し、がん細胞の増殖を防止することがわかりました。
これらからDHAが豊富に含まれている食物の補給は膵臓がんの発症を予防する可能性があることが分かりました。
*1. アポトーシス…プログラムされた細胞死。
*2. 血管新生…新しい血管が作られること。血管がないと酸素や栄養が足りなく腫瘍は一定以上のサイズにはなりませんが血管新生をすることでそれらを補い増殖、浸潤、転移を起こします。
詳しい内容は以下に記載致しますのでご興味のある方はどうぞご覧くださいませ。
<オメガ3脂肪酸(EPA/DHA)とは>
オメガ3脂肪酸(EPA/DHA) は、消費者庁がサプリメント11品目を評価した結果唯一 A評価を受け、その効果についての科学的根拠を有することが認められています。
これは平成24年4月に「食品の機能性評価モデル事業」という題で消費者庁より公表された全81ページにも及ぶ報告書です。
心血管疾患リスク低減、血中中性脂肪低下作用、関節炎や関節痛の代表として関節リウマチ症状緩和に対してA評価を与えました。
そして、現在はオメガ3脂肪酸の DPA ETA などの研究結果が続々と精度の高い論文として発表され、 EPA DHAと同様もしくはそれ以上の機能を発揮することが明かされています。
<これまでのオメガ3脂肪酸の研究>
◎オメガ3脂肪酸の高い消費が膵臓がんのリスクを低下させると示唆。
◎食餌性魚油の補給は動物モデルにおける膵臓がんの発症を抑制することが示唆。
◎DHAは抗腫瘍活性を示す。
上述のことが様々な研究より証明されてきました。既にDHA・EPAが結腸、乳房、前立腺がんにおける腫瘍脈管形成を阻害し治療に役立つ可能をゆうすることもわかっています。
また人の肝臓がん細胞、胃がん細胞でアポトーシス(*3)を起こす事も確認されています。
*3.アポトーシス…プログラムされた細胞死
<膵臓がんとは>
遺伝的な要因がかなり大きい。
膵臓がん細胞はアポトーシスに対する耐性を示すので=治療に対する耐性となり進行が促進する。
局所浸潤と転移のリスクが高いため長期生存率が低くなる。
腫瘍の増殖は血管新生(*2)に依存する。
<実験方法>
オメガ6脂肪酸とオメガ3脂肪酸をオメガ3多価不飽和脂肪酸(*4)に変換可能なマウスと、変換のできないマウスを観察。
その後
それらのマウスでオメガ3多価不飽和脂肪酸が膵臓上皮内新生物(PanIN)に及ぼす影響とそれが膵管腺癌(PDAC)へ進行する影響を確認した。
<結果>
他の脂肪酸をオメガ3多価不飽和脂肪酸に変換可能なマウスは変換ができないマウスに比べ
オメガ3多価不飽和脂肪酸濃度がはるかに高く、
膵癌腺癌(PDAC)の発生率が劇的に減少し、
癌腫や膵臓上皮内新生物(PanIN)などの病変を有する膵管が激減 した。
更に…
DHAとEPAは膵臓がん細胞の増殖を阻害しアポトーシスを誘導する
DHAは炎症誘発物質の産生を阻害することにより浸潤を抑える
DHA・EPAは強力な抗血管新生作用を有する ことが確認された。
<結論>
DHAは膵臓がん細胞においてアポトーシスを誘導する。
DHAは血管新生促進因子の発言を抑制し、がん細胞の増殖を防止する。
つまり、DHAが豊富に含まれる食物の補給は膵臓がんの発症の予防や治療に役立つ可能性が十分にあることがわかった。
- 2018.04.25
- 14:34
- コメント (0)
アルツハイマー病患者及びラットにおける記憶に対するホスファチジルセリンの影響
今回は2005年に発表された
(論題)
Effect of phosphatidyleserine on memory in patients and rats with Alzheimer's disease
(論題訳)
アルツハイマー病患者及びラットにおける記憶に対するホスファチジルセリン(PS)の影響
という論文をご紹介いたします。
この研究は
アルツハイマー病(以下AD)罹患患者には、コリン作動性神経伝達物質(*1)を増強する薬は維持管理のためにのみ使われ有効性は不十分であること、治療薬は現在ないがADの症状を遅延・改善させたい
上記の考えから行われました。
*1.コリン作動性神経伝達物質…神経刺激を伝える物質
この実験により
ホスファチジルセリン(PS)の経口摂取は重度の記憶障害を有するAD患者でも電話番号を覚え、誤っていたことを思い出し読書や話・作業中の注意が大幅に改善されることが分かりました。
詳しい内容は以下に記載致しますのでご興味のある方はどうぞご覧くださいませ。
<研究対象者・ラットと施した処置>
・AD患者
対照群(*2):25人→通常のAD治療、血圧血糖コントロール
観察群:32人→上記+ホスファチジルセリン(以下PS)300mg 1回/日を20週間経口投与
*2.対照群…処理を加える観察群と比較するための対照群(この場合PSを投与しない群)
・ADラット
高PS投与群:30mg/kg
低PS投与群:15mg/kg
対照群:PSの代わりに蒸留水
<処置前後の変化の確認方法>
・AD患者
語彙・画像マッチングスコアの確認
・ADラット
モリス水迷路試験(*3)・脳内のSOD(*4)活性
ヒドロキシラジカル(*5)阻害率・ChE(*6)レベル検出
*3.モリス水迷路…一箇所だけ浅くなっている水槽に不透明な水を入れラットをそこに泳がせる。
繰り返すことで周りの景色から浅瀬の位置を記憶し浅瀬へ到達する時間が短くなっていく。
*4.SOD…活性酸素を除去する抗酸化物質(多いと良い)
*5.ヒドロキシラジカル…OH。酸化物質(多いと良くない)
*6.ChE(コリンエステラーゼ)…神経伝達物質のAch(アセチルコリン)を分解(多いと良くない)
<AD発症のメカニズムと改善>
酸化物質により損傷された脳細胞が過酸化すること・それによる明らかな炎症反応・
アセチルコリンの増加に関連するのは明らかと言われている。
その為酸化物質を減らす・アセチルコリンを分解してしまうChEを減らす・
SOD等抗酸化物質を増やしてあげる事が改善につながる。
<結果>
PSの経口投与でAD患者では記憶機能等の明らかな改善が認められた。
人では確認できない為、ADラットで組織等を調べた結果上記で述べた改善方法のChEの減少・SOD(抗酸化物質)が増加しヒドロキシルラジカル(活性酸素)の抑制速度が改善され海馬(*7)の炎症の改善が認められた。
*7.海馬…長期記憶の形成に関係している脳の部分。ADの際海馬の萎縮が確認される。